南昌大学万昊教授等 | 乳酸乳球菌的单菌包埋技术及在胃肠道环境中的性能评价
本期介绍南昌大学万昊教授等发表在《中国食品学报》第24卷第4期青年论坛专刊特约专栏上的文章《乳酸乳球菌的单菌包埋技术及在胃肠道环境中的性能评价》。
背景及目的
目前,有多种方法可以帮助益生菌在口服过程中存活和繁衍,并提高益生菌的肠道定殖效率,如挤出[6]、冷冻干燥[7]、喷雾干燥[8]和微胶囊化[9]等。这些方法虽然在一定程度上提升了益生菌在肠道中的活性,但是存在操作复杂、产率低等问题,同时可能对益生菌造成机械损伤[10]。因此,迫切需要找到一种简单有效的方法来包埋益生菌,以增强益生菌对胃肠道环境应激的抵抗能力,延长益生菌在肠道的滞留时间,提高益生菌定殖率,达到更好地发挥益生菌在体内效能的目的。
β-葡聚糖(GN)是一种常见的益生元,广泛存在于大麦、小麦和燕麦等天然植物中[12],可被肠道菌群代谢为短链脂肪酸,表现出丰富的生理活性,如改善肠道环境,增加肠道菌群丰度和修复肠道屏障等[13]。除了优越的生物活性,GN的大孔蜂窝状结构,可以比任何其它壁材更有效地捕获微生物。由于GN在上消化道稳定[14],可以减轻益生菌在进入肠道过程中失活的风险,提高益生菌的存活率,并将益生菌高浓度地输送到指定部位,因此现已作为益生菌包埋壁材使用[15]。然而,GN存在黏度大、溶解性差等问题[17]。羧甲基化β-葡聚糖(mGN)在不改变GN空间结构的同时,在很大程度上解决了其难溶于水的问题,并提升了GN的生物活性[18]。然而,mGN无法直接黏附在单个益生菌的表面对其进行保护。寻找到能够连接内层益生菌与壁材mGN的“桥梁”,是实现mGN对单个益生菌包埋的关键。金属-酚醛网络是由酚类配体(如单宁酸)和金属离子(如Fe3+)组成的超分子复合物,可通过一步法简便地组装成配位络合物,并黏附在多种材料表面[19]。酚类物质具有较多羟基和较高的黏附能力,可通过氢键作用将mGN吸附到金属-酚醛网络结构的表面,达到mGN对益生菌包埋的目的。
乳酸乳球菌(Lactococcus lactis,LL)是乳酸菌属中的一种重要模式菌,同样也是食品级微生物(Generally regards as safe,GRAS),被广泛应用于食品工业[20]。LL具有促进消化,维持肠胃菌群平衡,提高宿主免疫力和加固肠道黏膜等作用[21]。然而,关于乳酸乳球菌包埋的研究较少,而包埋单个乳酸乳球菌的研究更鲜见报道。基于此,本研究以mGN作为壁材,通过金属-酚醛网络的桥联作用,将mGN黏附在LL表面,旨在探究其对所包埋的LL胃肠道耐受性及肠道滞留能力的影响。
研究方法
使用羧甲基化β-葡聚糖(mGN),通过金属-酚醛网络结构(Fe-TA)的桥联作用,将其黏附在乳酸乳球菌(LL)表面,构建乳酸乳球菌的包埋体系LL@Fe-TA@mGN,并评价LL@Fe-TA@mGN对胃液与胆盐的抗性及其在体内的滞留能力。
研究结果
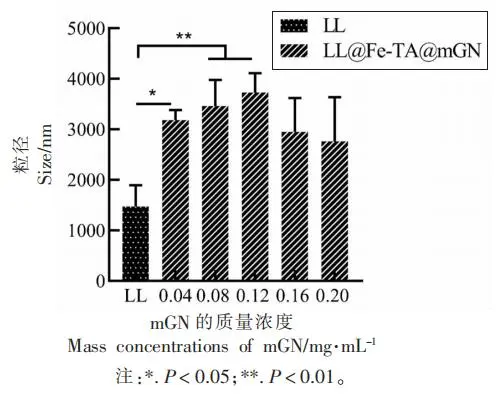
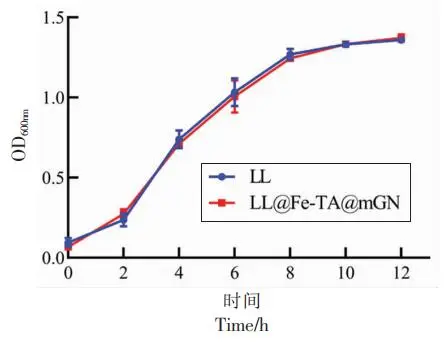
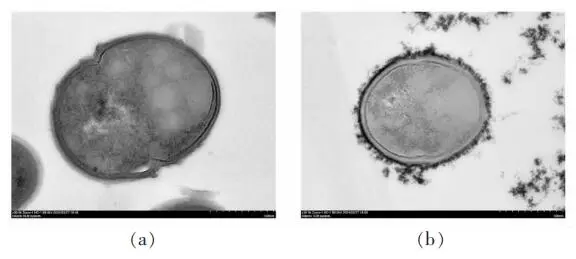
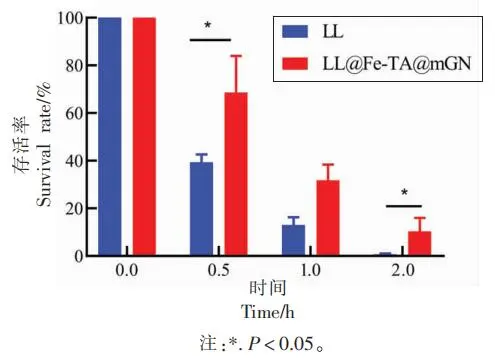
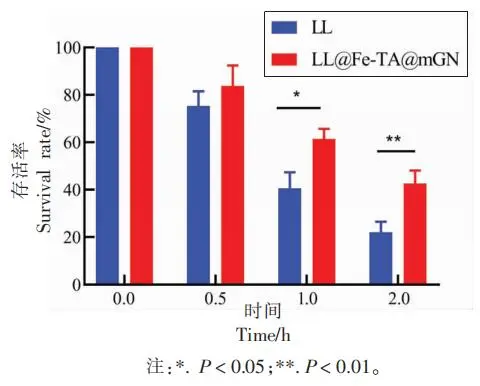
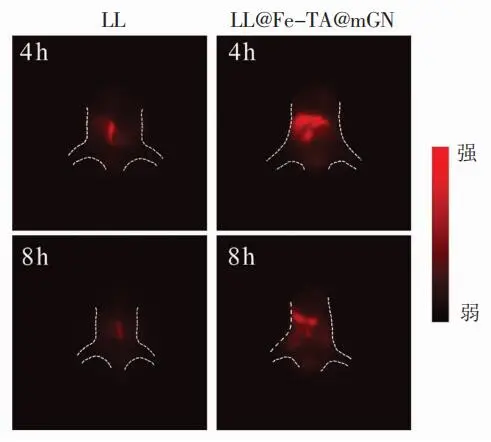
当mGN的质量浓度为0.12 mg/mL时,LL@Fe-TA@mGN体系的粒径和zeta-电位都达到峰值,表明该质量浓度为mGN包埋单个乳酸乳球菌的最佳质量浓度。在MRS液体培养基中,LL@Fe-TA@mGN的生长曲线与LL的生长曲线没有显著性差异,说明mGN的毒性可以忽略不计。在扫描电镜与透射电镜分析中均可清晰地看到一层“膜”完整地包覆在乳酸乳球菌表面。经2 h模拟胃液与胆盐的孵育,mGN包埋后的LL抗胃液能力与抗胆盐能力相比于未包埋的LL分别提升14.63倍与1.94倍。体内荧光成像实验证实LL@Fe-TA@mGN具有更强的肠道滞留能力。
图1 包埋过程中使用的mGN质量浓度(0~0.2 mg/mL)对LL@Fe-TA@mGN粒径的影响
图2 包埋过程中mGN质量浓度(0~0.2 mg/mL)对LL@Fe-TA@mGN zeta-电位的影响
图3 LL与LL@Fe-TA@mGN的生长曲线 图4 LL(a)与LL@Fe-TA@mGN(b)的SEM图(×30k) 图5 LL(a)与LL@Fe-TA@mGN(b)的TEM图(×30k) 图6 LL与LL@Fe-TA@mGN暴露在模拟胃液(pH 2.5)中的存活率 图7 LL与LL@Fe-TA@mGN暴露在胆盐中的存活率 图8 小鼠灌胃Cy-5标记的LL或者LL@Fe-TA@mGN后的体内成像 研究结论 以羧甲基化β-葡聚糖为壁材,通过金属-酚醛网络结构的桥联作用,可实现对单个乳酸乳球菌的完整包埋。这种包埋方法简单、快速,在不改变乳酸乳球菌自身结构的情况下,可显著提升乳酸乳球菌的抗胃液与抗胆盐能力,并延长其在体内的滞留,从而帮助乳酸乳球菌在体内更好地繁殖。研究结果为乳酸乳球菌包埋体系的构建提供了新思路,并为提高乳酸乳球菌在胃肠道的活性提供了理论依据。 作者简介 万昊,国家海外高层次人才引进计划青年项目入选者,江西省杰青。南昌大学食品科学与资源挖掘全国重点实验室教授,食品学院教授,博士生和硕士生导师。主持国家自然科学基金面上项目、国家自然科学基金青年项目、江西省杰出青年基金、江西省国家级高层次人才创新创业基金和江西省重点项目基金。在食品科学、分析科学、生命科学、材料化学等领域开展了前沿性的基础交叉研究,并注重将科学研究与改善人体健康密切关联。其研究方向主要集中在以下两个方面:食品功能因子的稳态化及其精准递送和生物仿生载体的构建及其在疾病治疗中的应用。截至2023年为止,以第一作者和共同第一作者或通讯作者身份在高水平期刊上发表多篇学术论文,包括《Nature Methods》、《Nature Communications》、《PNAS》、《Advanced Materials》、《ACS Nano》、《Advanced Functional Materials》、《Advanced Science》、《Food Chemistry》和《Advanced Healthcare Materials》等,论文总引用4874次。 来源:中国食品学报
者简介作