南昌大学食品学院聂少平教授团队重要成果:益生元赋能益生菌增强胃肠道耐受性并实现靶向结肠释放协同缓解结肠炎
南昌大学食品学院聂少平教授团队重要成果:益生元赋能益生菌增强胃肠道耐受性并实现靶向结肠释放协同缓解结肠炎
近期,南昌大学食品科学与资源挖掘全国重点实验室聂少平教授课题组国际权威期刊《Journal of Controlled Release》(Q1,中科院1区TOP,IF: 10.5)发表题为“Prebiotics empower probiotics with gastrointestinal stress resistance for colon-targeted release to synergistically alleviate colitis”的研究性论文。本文第一作者为南昌大学博士研究生嵇海华,万昊教授和聂少平教授为通讯作者。文章提出了一种基于生物正交化学的单细胞逐层包裹策略,通过将β-葡聚糖(GN)益生元包裹于植物乳杆菌(Lp)表面,显著增强其胃肠道生存能力,实现靶向结肠的释放,并协同缓解溃疡性结肠炎(UC)。

研究背景
溃疡性结肠炎(UC)是一种全球性的疾病,其特征是非特异性炎症,对人类健康构成严重威胁。目前,5-氨基水杨酸、糖皮质激素和免疫抑制剂等药物是治疗UC的主流方法,但由于疗效低、副作用严重、费用高和患者依从性差等问题,研究人员正努力探索替代治疗方法。
益生菌作为一类对宿主健康有益的微生物,因其生活方式友好、非侵入性的口服模式、较少的副作用和低成本等特点,被广泛接受为多种疾病的治疗手段。特别是,益生菌在缓解UC方面显示出极大的治疗潜力。例如,大肠杆菌Nissle 1917(EcN)已被证明可以通过丰富有益肠道菌群来改善葡聚糖硫酸钠(DSS)诱导的结肠损伤。同样,植物乳杆菌(Lp)菌株也被发现通过积极调节肠道菌群、改善肠道完整性和调节免疫反应来缓解UC症状。然而,口服益生菌不可避免地会遭遇恶劣的胃肠道环境(如胃酸、蛋白水解酶和胆盐)的挑战,导致到达结肠的活性益生菌数量不足,从而严重削弱其治疗UC的效果。因此,保护益生菌免受胃肠道挑战以确保其能够靶向递送至结肠是增强益生菌治疗效果的关键步骤。
为了保护益生菌免受胃肠道损害,将益生菌包裹在基质中的方法是一种直接的方式,包括挤出、乳化和喷雾干燥方法。然而,这些方法虽然提高了益生菌对胃肠道应激的耐受性,但也不可避免地对益生菌造成物理损伤,并且由于不是单细胞水平的包裹方式,其保护效果有限。相比之下,逐层组装的包裹策略展示了更强的保护效果,特别是在通过共价键形成的更加稳定和紧凑的结构时。然而,现有研究很少实现益生菌的共价逐层包裹,这主要是因为益生菌的脆弱特性与大多数化学反应不相容。受诺贝尔奖相关研究启发,生物正交化学利用内源性生物合成机制将非天然前体同化以生成化学标记(如叠氮基),并通过位点特异性共价结合实现后续分子修饰。结合逐层组装策略,生物正交化学有望用于构建保护层以保护益生菌。
在此研究中,我们通过生物正交逐层包覆策略,将β-葡聚糖(GN)作为保护层材料应用于植物乳杆菌(Lp),并验证了该策略对改善益生菌在胃肠道环境中的生存能力以及在结肠的靶向释放和协同治疗UC的效果。
结论与展望
本研究通过将益生元(β-葡聚糖,GN)与益生菌(植物乳杆菌,Lp)结合,提出了一种新颖的基于生物正交化学的逐层包覆策略(Lp@CGN),为改善益生菌在胃肠道环境中的存活率以及在结肠的靶向释放提供了新方法。研究表明:Lp@CGN的“盾牌”显著增强了益生菌在胃酸、消化酶和胆盐等胃肠道应激条件下的耐受性,其存活率提高了约276倍。到达结肠后,GN“盾牌”在肠道菌群的作用下被代谢为短链脂肪酸(SCFAs),同时释放益生菌发挥其益生功能。Lp@CGN在溃疡性结肠炎(UC)预防和治疗模型中表现出显著效果,包括修复肠道黏膜屏障、调节炎症因子、改善肠道菌群失衡和促进SCFAs生成。这一研究验证了利用化学工具重构益生菌的可行性,为提升益生菌在疾病治疗中的应用潜力提供了重要的理论和技术支持。
图文摘要
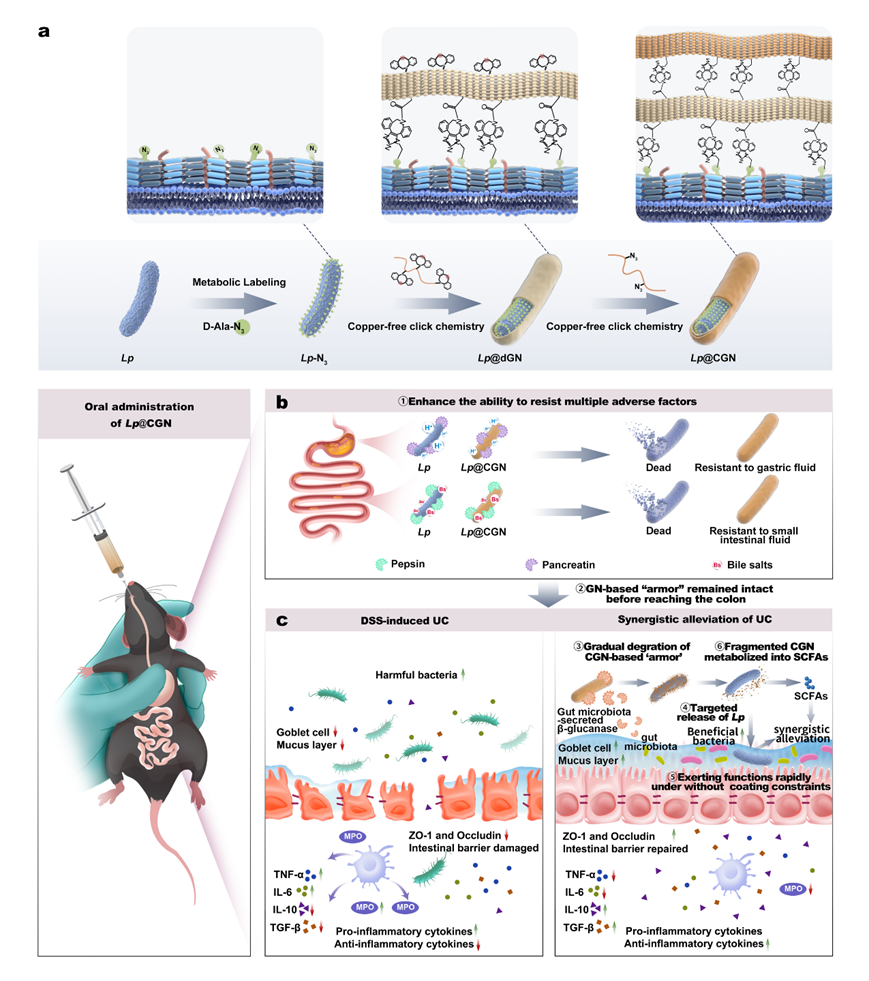
图1.Lp@CGN的制备及其缓解小鼠DSS诱导的溃疡性结肠炎的过程示意图。(a)通过生物正交逐层包覆策略制备Lp@CGN的合成步骤示意;(b) 具有结肠靶向降解特性的 GN“盾牌”在口服给药后提高益生菌存活率并有效递送至结肠;(c) Lp@CGN缓解溃疡性结肠炎的潜在机制示意:GN的逐层包覆对胃酸、消化酶和胆盐等胃肠道应激表现出优异的保护效果,保持结构完整直到到达结肠。GN“盾牌”在结肠被肠道菌群代谢为短链脂肪酸(SCFAs),同时释放益生菌Lp,协同发挥治疗作用。
原文链接
https://doi.org/10.1016/j.jconrel.2025.01.059
通讯作者简介

聂少平,教授,博导,南昌大学党委常委、副校长,国家高层次人才特殊支持计划领军人才,国家自然科学基金杰青、优青项目获得者,科技部创新人才推进计划中青年科技创新领军人才,教育部“新世纪优秀人才支持计划”入选者,江西省主要学科学术带头人,江西省百千万人才工程,享受国务院政府特殊津贴专家。兼任国务院第八届学位委员会食品科学与工程学科评议组成员,全国食品与营养专业学位研究生教育指导委员会委员,Journal of Agricultural and Food Chemistry副主编,Food Frontiers创刊主编,Food Science and Human Wellness、《中国食品学报》等杂志的编委,中国食品科学技术学会理事会理事等。主要从事食品化学与营养学、食品安全与分析,特别是食品复杂碳水化合物(主要为生物活性多糖和膳食纤维)、食物组分与营养健康精准调控等领域的研究与新产品创制,主持国家自然科学基金重点项目以及国家重点研发计划项目等各类项目30多项,以第一或通讯作者(含共同)发表高质量学术论文300多篇,h-index为73;主编中英文著作7部;授权发明专利45件,多次入选科睿唯安全球“高被引科学家”、爱思唯尔中国高被引学者等。获国家级科技进步奖二等奖2项、江西省自然科学奖一等奖2项、江西省科技进步奖一等奖2项、教育部自然科学二等奖1项、国家级教学成果奖二等奖2项、江西省教学成果奖一等奖1项等各类奖励10多项。

万昊,教授,博导,国家海外高层次人才引进计划青年项目入选者,江西省杰青。南昌大学食品科学与资源挖掘全国重点实验室教授,食品学院教授,博士生和硕士生导师。主持国家自然科学基金面上项目、国家自然科学基金青年项目、江西省杰出青年基金、江西省国家级高层次人才创新创业基金和江西省重点项目基金。担任国际著名SCI学术期刊审稿人,包括Analytical Chemistry、ACS Applied Materials & Interface、Theranostics、Carbon、Analytica Chimica Acta等。在食品科学、分析科学、生命科学、材料化学等领域开展了前沿性的基础交叉研究,并注重将科学研究与改善人体健康密切关联。其研究方向主要集中在以下几个方面:食品功能因子的稳态化及其精准递送;食品蛋白质组学;功能化纳米颗粒的构建及其在癌症精准治疗中的应用;生物仿生载体的构建及其在疾病治疗中的应用。截至2023年为止,以第一作者和共同第一作者或通讯作者身份在高水平期刊上发表22篇学术论文,包括Nature Methods、Nature Communications、PNAS、Advanced Materials、ACS Nano、Advanced Functional Materials、Food Chemistry和Advanced Healthcare Materials等;以共同作者身份参与发表20篇学术论文,包括Nature Medicine、Nature Biotechnology、Nano Today、Chemical Science等。论文总引用4247次。申请和授权专利7项,其中包括3件国外专利。
第一作者简介

嵇海华,南昌大学食品学院2021级博士研究生,研究方向为食品功能因子的稳态化及其精准递送。以第一作者/共同一作在Biomaterials、Journal of Controlled Release、ACS Nano、Food & Function等国际期刊发表SCI论文5篇,申请专利7项,已授权专利5项。荣获2022年度中国食品科技十大进展(首届),江西省研究生“十佳实践之星”。