审阅︱辛洪波
责编︱王思珍
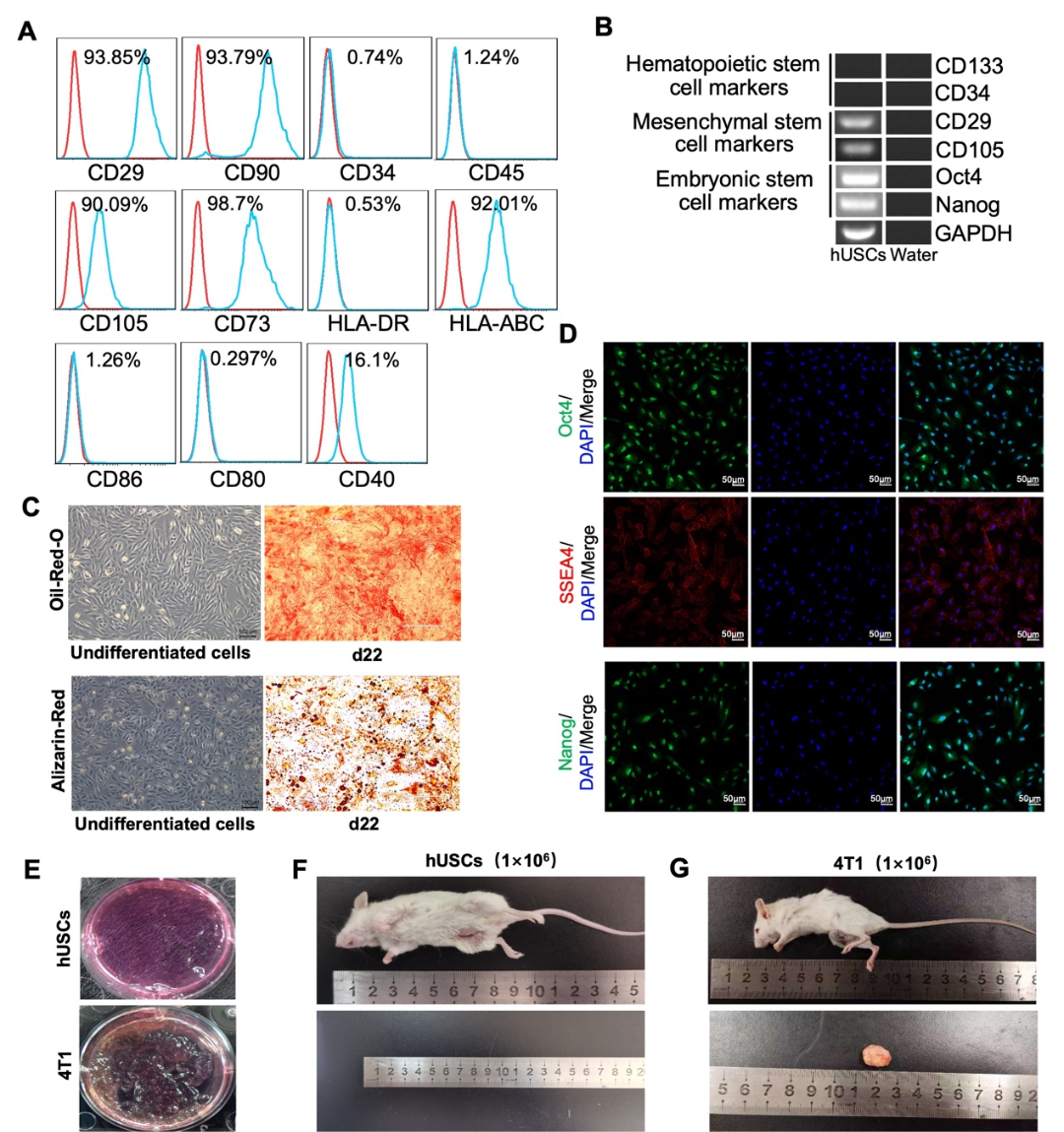
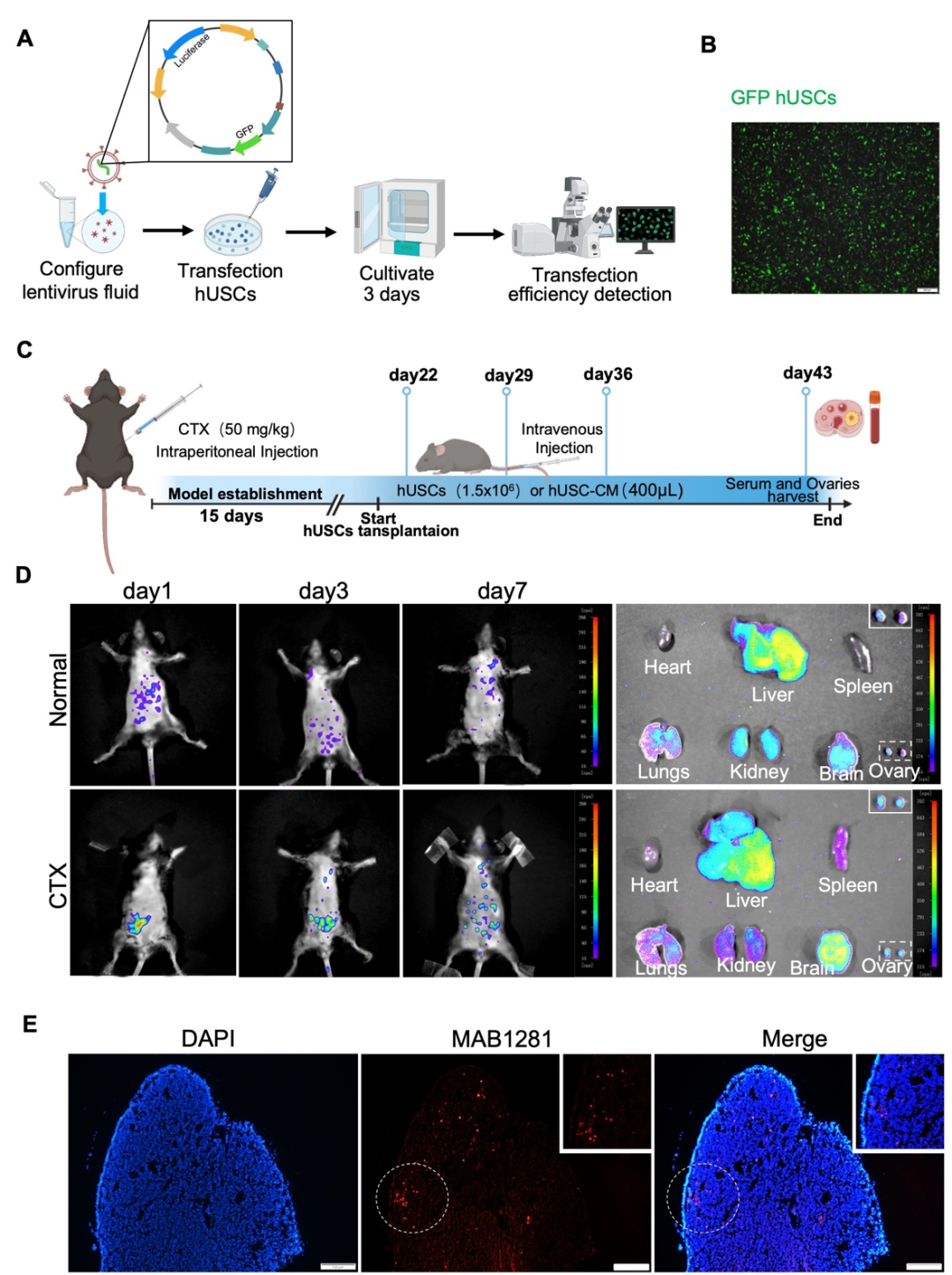
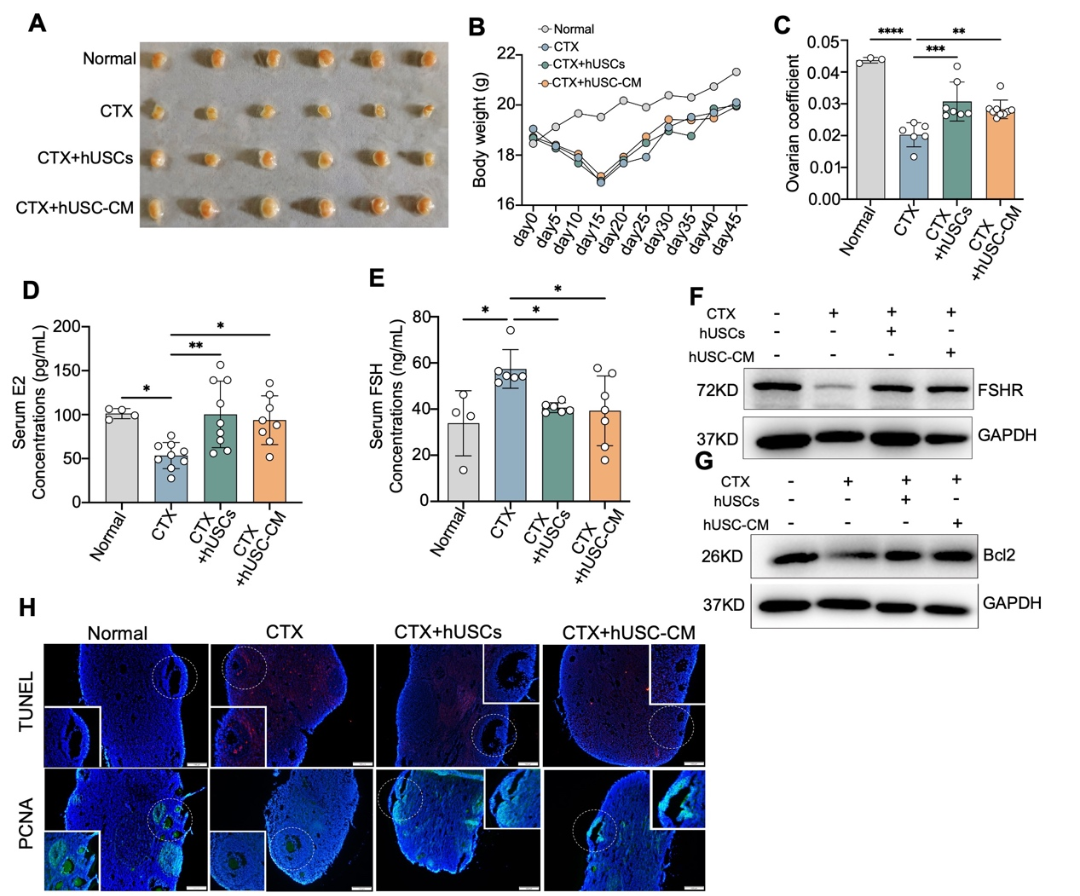
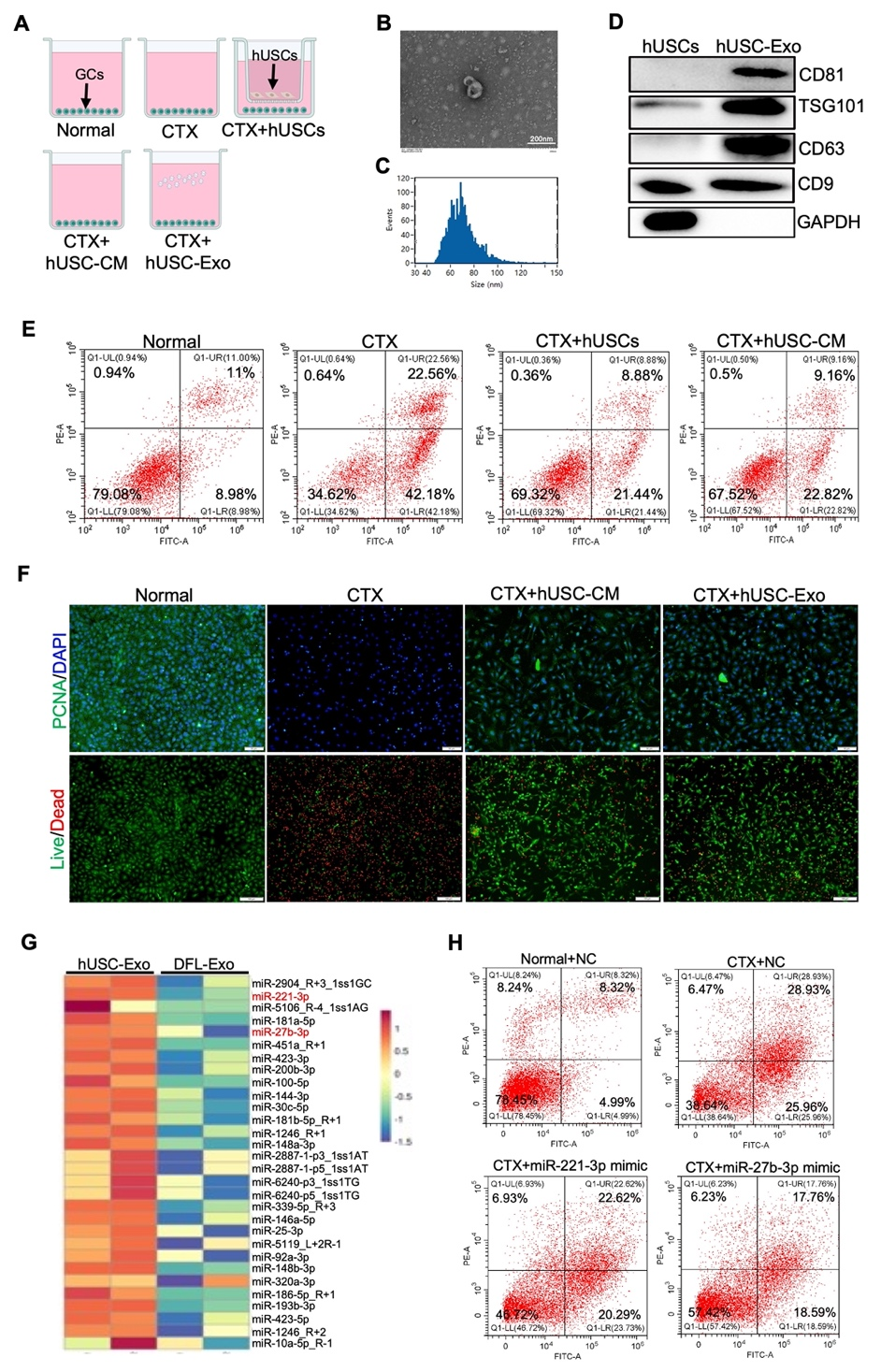
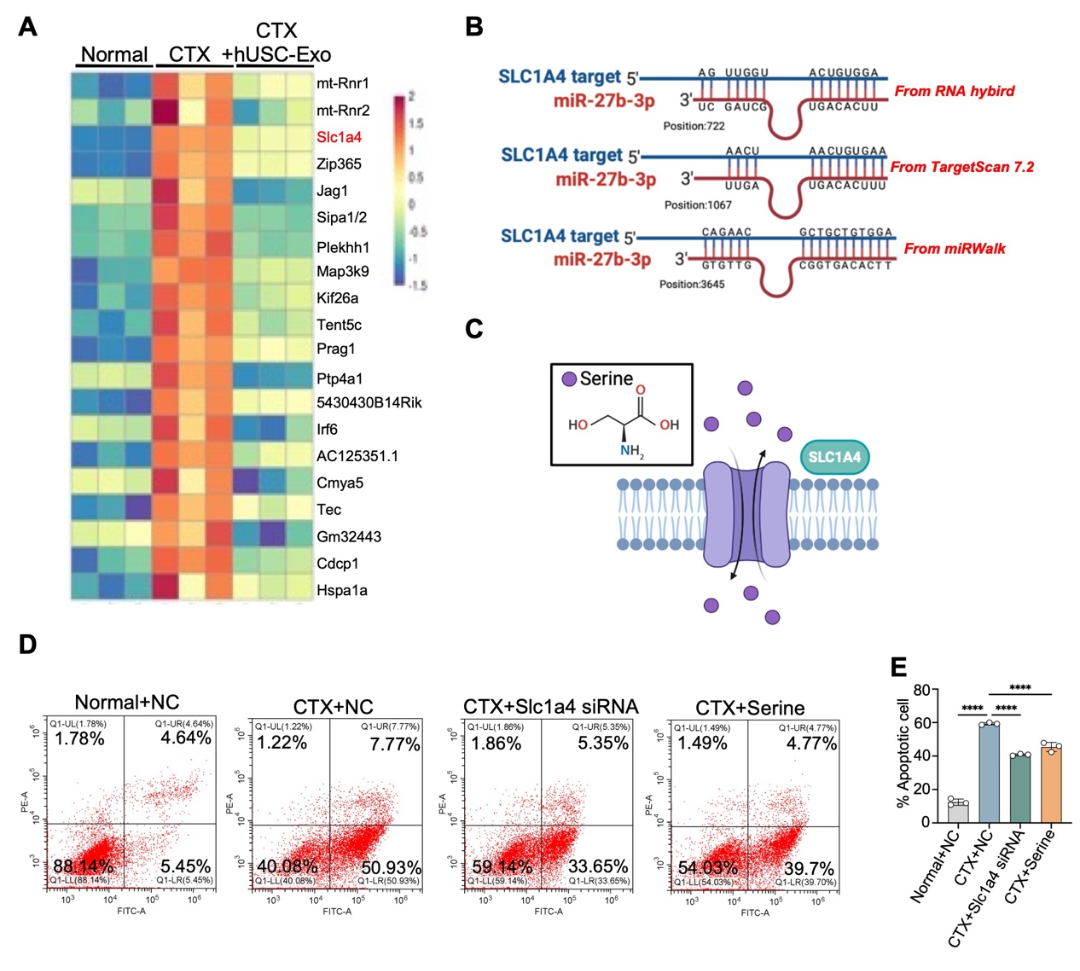
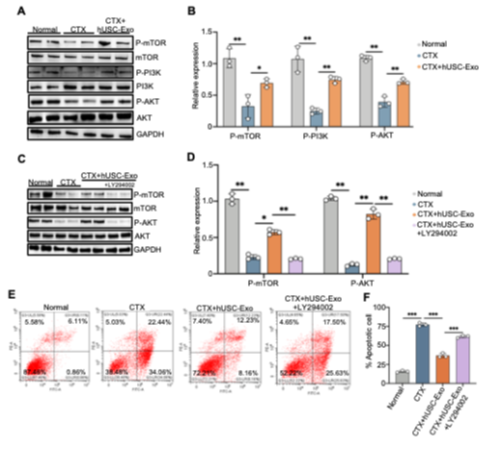
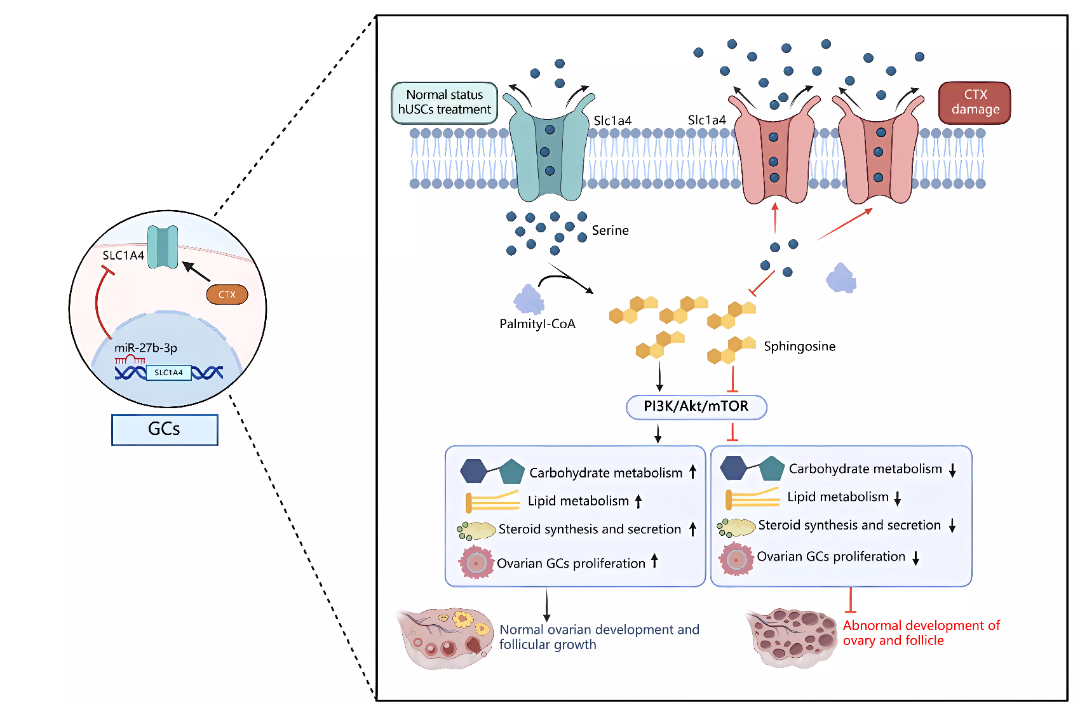
卵巢早衰(POF)作为卵巢的一种功能性缺陷,严重影响女性的身心健康,并伴随着高血压、骨质疏松、不孕、心血管疾病、心理障碍等多种严重后果。环磷酰胺(CTX)诱导的POF是乳腺癌化疗中最常见的副作用,发生率高达40%。卵巢颗粒细胞(GCs)是卵巢中分泌性激素的主要功能细胞,卵巢中GCs凋亡导致了卵泡的萎缩和闭锁最终导致卵巢功能的缺失。然而,令人遗憾的是由于CTX诱导卵巢早衰的机制尚不清楚,目前临床上缺乏有效预防和治疗CTX引起的卵巢早衰的方法。因此,寻找一种新的治疗方法来延缓或治疗CTX诱导的POF并阐述其具体分子机制是非常必要和迫切的。人尿源性干细胞(hUSCs)是一种新型的干细胞亚群,具有高度的自我更新、增殖、多向分化能力等优点,且易于从尿液中获得。更加值得关注的是,hUSCs具备自体移植的可能性,可减少应用hUSCs时的伦理障碍。现有研究表明,hUSCs对许多疾病具有治疗潜力,例如膀胱修复、勃起功能障碍、糖尿病、软骨缺损、皮肤损伤和急性肾损伤。然而,hUSCs在POF中的作用和机制尚未得到探讨。SLC1A4是一种中性氨基酸转运蛋白,负责哺乳动物细胞中四种中性氨基酸(如半胱氨酸、丝氨酸、甘氨酸和丙氨酸)的转运,其也是哺乳动物体内最主要的丝氨酸转运体。丝氨酸在细胞生长、器官发育以及细胞、神经元、干细胞、肌肉细胞和免疫细胞增殖所涉及的各种生化过程中起着至关重要的作用。研究表明,在许多神经系统疾病中,SLC1A4的表达失调伴随着神经细胞的细胞内丝氨酸水平的降低,从而影响神经系统的正常生长和发育。然而,SLC1A4通过调节丝氨酸的转运在POF疾病中的潜在作用尚未见任何报道。因此,本研究旨在探讨环磷酰胺诱导的卵巢早衰的机制及人USCs对环磷酰胺诱导的卵巢早衰的治疗作用。近日,南昌大学转化医学研究院辛洪波教授团队在Cellular & Molecular Biology Letters上发表题为“Human urine stem cells protect against cyclophosphamide-induced premature ovarian failure by inhibiting SLC1A4-mediated outfux of intracellular serine in ovarian granulosa cells”的研究。该研究首先发现hUSCs表达间充质干细胞及胚胎干细胞表面标志物,不表达造血干细胞表面标志物,体外内成瘤性研究显示,hUSCs不具有致瘤性。进一步的体内研究显示,hUSCs及其条件培养基(hUSC-CM)可以显著抑制CTX引起的卵巢萎缩、雌激素及促卵泡素分泌紊乱以及闭锁卵泡的增加。深入的分析发现,hUSCs及hUSC-CM主要靶向作用于GCs,抑制了CTX引起的GCs凋亡并促进其增殖。此外,体外研究还揭示了hUSCs发挥治疗CTX引起POF的关键物质为外泌体(hUSC-Exo),并分离提取得到了hUSC-Exo。机制研究发现,CTX导致了GCs内SLC1A4的高表达进而导致GCs内丝氨酸外排而引起低丝氨酸的现象,hUSC-Exo中miRNA-27b-3p可以与GCs内SLC1A4的3’-UTR区域结合,抑制CTX引起的SLC1A4表达升高维持GCs内丝氨酸的平衡,从而激活PI3K/Akt/mTOR信号通路,减少CTX引起的GCs凋亡。基于这些发现,研究者提出了包含SLC1A4及丝氨酸参与的POF的全新分子机制。首先研究者检测了hUSCs表面标志物、基因表达、成骨成脂分化及体内外致瘤性,结果显示hUSCs表达间充质干细胞及胚胎干细胞表面标志物及基因,不表达造血干细胞表面标志物及基因。体外可向脂肪细胞及骨细胞分化,且不具有致瘤性。接下来研究者将带有GFP及荧光素酶基因的慢病毒转染至hUSCs中,通过尾静脉移植至小鼠体内,结果显示hUSCs可以向受损卵巢区域富集,且在最后一次移植的7天后,卵巢组织中仍然可以检测到hUSCs的驻留(MAB1281为人细胞核特异性抗体)。进一步的动物研究发现,hUSCs及hUSC-CM的移植显著抑制了CTX引起的卵巢的萎缩,并显著改善了CTX引起的性激素分泌紊乱现象。值得注意的是,CTX导致卵巢萎缩及性激素分泌紊乱主要是靶向GCs导致,Western blot、TUNEL及PCNA免疫荧光的结果显示,hUSCs及hUSC-CM的移植抑制了CTX诱导的GCs凋亡,提示GCs的正常活性及功能是维持卵巢健康的关键。图3. hUSCs及hUSC-CM移植通过减少GCs的凋亡改善CTX引起的POF接下来,体外Annexin V/PI染色及细胞活死染色分析揭示,hUSCs主要是通过旁分泌外泌体抑制了CTX引起的GCs凋亡。研究者进一步提取了hUSCs的外泌体,通过miRNA测序发现miRNA-27b-3p及miRNA-221-3p有显著的差异表达(DFL-Exo作为阴性对照)。值得注意的是,在GCs中过表达miRNA-27b-3p及miRNA-221-3p可以抑制CTX引起的GCs凋亡,其中miRNA-27b-3p的效果最为显著,提示miRNA-27b-3p可能在其中起到关键作用。图4. hUSCs通过旁分泌外泌体中miRNA-27b-3p抑制CTX引起的GCs凋亡在明确上游具体miRNA后,研究者进行了进一步的机制探究,该团队通过GCs的转录组测序发现CTX可以导致GCs细胞内SLC1A4表达的显著上调。miRNA与靶基因结合位点预测的结果提示,miRNA-27b-3p与SLC1A4存在多个结合位点。结合SLC1A4对于丝氨酸转运的功能,研究者在GCs中敲低SLC1A4的表达及补充丝氨酸均可以有效抑制CTX引起的GCs凋亡。基于上述发现研究者推断,hUSC-Exo中的miRNA-27b-3p可靶向结合至GCs的SLC1A4基因3’-UTR区抑制CTX引起的SLC1A4表达增加,进而维持GCs细胞内丝氨酸水平的稳定,从而抑制GCs凋亡。图5. SLC1A4敲低通过抑制细胞内丝氨酸的流出抑制CTX引起的GCs凋亡最后,Western blot的实验证实,hUSC-Exo主要通过调节GCs细胞内PI3K/Akt/mTOR信号通路抑制GCs的凋亡。当加入该信号通路抑制剂LY294002抑制PI3K/Akt/mTOR信号通路后,原本hUSC-Exo抑制CTX引起GCs凋亡的效果也显著下降。图6. hUSC-Exo通过激活PI3K/Akt/mTOR信号通路抑制CTX诱导的GCs凋亡综上所述,研究者证实了CTX诱导的GCs凋亡是卵巢POF发生的关键,CTX通过增加GCs中SLC1A4的表达降低了细胞内丝氨酸水平,进而通过抑制PI3K/Akt/mTOR信号通路促进了GCs凋亡,最终导致POF的发生。hUSCs对CTX诱导的POF的保护作用的潜在机制与hUSC-Exo中的miRNA-27b-3p有关,其通过特异性靶向GCs中的SLC1A4调节GCs内丝氨酸的水平进而抑制GCs凋亡并促进卵巢正常生长。GCs内升高的丝氨酸通过激活PI3K/Akt/mTOR信号通路而改善CTX引起的POF。此外,这项研究提示,基于hUSCs的细胞治疗方法或单纯性补充丝氨酸可能是临床上预防和治疗POF的有效措施。
原文链接:https://cmbl.biomedcentral.com/articles/10.1186/s11658-025-00701-1南昌大学生命科学学院顾皓铖博士与南昌大学转化医学研究院汪玲芳助理研究员为共同第一作者;南昌大学转化医学研究院邓柯玉教授与辛洪波教授为共同通讯作者。该研究获得国家重点研发计划(编号:2022YFA1104300)、国家自然科学基金(编号:82470454,82470454,82270302,81970256,82160285,82000354)及江西省自然科学基金(编号:20212BCJ23043)资助。